Lesezeit: 11 Minuten
Daten der Versorgungsforschung in der Onkologie geben neben den Zulassungsstudien einen wichtigen und realen Input für die Behandlung der Patienten*innen in der täglichen Praxis. Mittlerweile hat sich die Immuntherapie in den meisten Tumorentitäten etabliert, sowohl als Monotherapie als auch in Kombination mit anderer Substanzen wie Targeted- und Chemotherapeutika. Gerade in der Uro-Onkologie hat sich das Behandlungsspektrum in den letzten Jahren deutlich erweitert und nahezu auf jedem internationalen Kongress werden neue Substanzen und Kombinationen präsentiert.
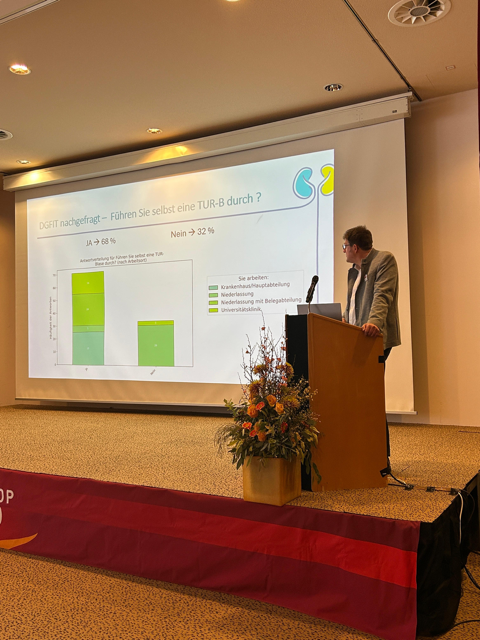
Auf dem Satellitensymposium der DGFIT auf dem Urologischen Winterworkshop 2026 in Leogang wurden neben verschiedenen Aspekten der Versorgungsforschung auch neue Daten der Uro-Onkologie vorgestellt. Das Symposium wurde von Prof. Dr. Michael Siebels (München) und Prof. Dr. Axel Hegele (Biedenkopf) moderiert.

Adjuvante Therapie des Nierenzellkarzinoms: Status quo im Jahr 2026
Prof. Dr. med. Christian Doehn, Urologikum Lübeck, Lübeck

Seit Jahrzehnten ist bekannt, dass nicht alle Patienten mit einem Nierenzellkarzinom durch die operative Tumorentfernung dauerhaft geheilt werden.
Seit Jahrzehnten wird daher die adjuvante Therapie in Studien untersucht. Vor mehr als 20 Jahren wurde in Deutschland eine Studie zu Wertigkeit einer autologen Tumorzellvakzine vorgenommen – es zeigte sich damals ein Vorteil im krankheitsfreien Überleben (DFS) für den Verumarm [1]. Dies war die erste positive Studie zur adjuvanten Therapie beim Nierenzellkarzinom überhaupt. Präklinische Daten unterstützen die Rationale für das Vorgehen [2]. Der EMA (damals EMEA) reichten die Daten seinerzeit nicht für eine Zulassung. Man forderte eine konfirmatorische Studie, zu der es nicht kam.
In den Folgejahren wurden quasi alle für die Systemtherapie des metastasiserten Nierenzellkarzinoms zugelassenen Medikamente (Tyrosinkinase-Inhibitoren, mTOR-Inhibitoren) auch im adjuvanten Einsatz geprüft – alle Studien waren negativ.
Im Jahr 2021 zeigte erstmals ein Checkpointinhibitor (Pembrolizumab) eine Verbesserung des DFS mit einer HR von 0,68 (und später auch des OS) gegenüber Plazebo bei Patienten mit einem Nierenzellkarzinom im Stadium T2G4 oder T3 oder/und N1 oder/und M1 (nach vollständiger Entfernung der Metastase, no evidence of disease, NED) [3]. Die adjuvante Therapie mit Pembrolizumab wurde im Jahr 2023 in Europa zugelassen. Die Real World zeigt, dass bevorzugt Patienten mit „höheren“ Tumorstadien (insbesondere M1 NED) adjuvant behandelt werden.
Beim ASCO-GU-Kongress 2026 wurden die Ergebnisse einer weiteren positiven Studie präsentiert [4]. Die Einschlußkriterien entsprachen denen der KN-564-Studie. In der LITESPARK-022-Studie erhielten die Patienten entweder den bisherigen Standard oder die Kombination aus Pembrolizumab und Belzutifan (ein Inhibitor des Hypoxieinduzierbaren Faktors-2α, HIF-2α). Die Kombinationstherapie zeigte dabei ein deutlich besseres DFS (HR 0,72) bei allerdings auch erhöhter Nebenwirkungs- und Abbruchrate.
Für das laufende Jahr ist noch nicht mit einer Zulassung der Kombinationstherapie zu rechnen. Bis dahin stellt Pembrolizumab den Standard der adjuvanten Therapie des Nierenzellkarzinoms dar. Die Diskussion um die Patientenselektion war noch gar nicht abgeschlossen und wird durch die Ergebnisse der Kombinationstherapie neue Fahrt aufnehmen. Die relevanten Therapiekosten dürften ein zusätzlicher Bestandteil dieser Diskussion werden. Kein Bestandteilt der Diskussion ist (seit mindestens 22 Jahren) die Notwendigkeit zur Durchführung konfirmatorischer Studien bei der adjuvanten Therapie des Nierenzellkarzinoms. Derartige Studien sind offenbar nämlich gar nicht mehr notwendig.
Literatur
- Jocham D, Richter A, Hoffmann L, Iwig K, Fahlenkamp D, Zakrzewski G, Schmitt E, Dannenberg T, Lehmacher W, von Wietersheim J, Doehn C. Adjuvant autologous renal tumour cell vaccine and risk of tumour progression in patients with renal-cell carcinoma after radical nephrectomy: phase III, randomised controlled trial. Lancet. 2004 Feb 21;363(9409):594-9.
- Doehn C, Esser N, Pauels HG, Kiessig ST, Stelljes M, Grossmann A, Jocham D, Drevs J. Mode-of-action, efficacy, and safety of a homologous multi-epitope vaccine in a murine model for adjuvant treatment of renal cell carcinoma. Eur Urol. 2009 Jul;56(1):123-31.
- Choueiri TK, Tomczak P, Park SH, Venugopal B, Ferguson T, Chang YH, Hajek J, Symeonides SN, Lee JL, Sarwar N, Thiery-Vuillemin A, Gross-Goupil M, Mahave M, Haas NB, Sawrycki P, Gurney H, Chevreau C, Melichar B, Kopyltsov E, Alva A, Burke JM, Doshi G, Topart D, Oudard S, Hammers H, Kitamura H, Bedke J, Perini RF, Zhang P, Imai K, Willemann-Rogerio J, Quinn DI, Powles T. Adjuvant Pembrolizumab after Nephrectomy in Renal-Cell Carcinoma. N Engl J Med. 2021 Aug 19;385(8):683-694.
- Choueiri TK, Motzer RJ, Karam JA, Ye D, He Z, Caglevic C, Yip W, Suarez C, Ferguson T, Chang WYH, Rojas C, Iacovelli R, Ürün Y, Verzoni E, Limon JCV, Porta C, Liu H, Sharma M, Burgents JE, Powles T. Adjuvant pembrolizumab plus belzutifan versus pembrolizumab for clear cell renal cell carcinoma (ccRCC): The randomized phase 3 LITESPARK-022 study. J Clin Oncol 44, LBA418(2026).
Aktuelle Diagnostik und Therapie verschiedener Stadien des Prostatakarzinoms – Real-World Daten einer deutschlandweiten Umfrage der Deutschen Gesellschaft für Immun- und Targeted Therapie (DGFIT)
Prof. Dr. A. Hegele, Biedenkopf

Einleitung
Für die Diagnostik sowie stadiengerechte Therapie des Prostatakarzinoms (PCA) existieren viele Optionen. Ziel der Befragung der Deutschen Gesellschaft für Immun- und Targeted-Therapie e.V. (DGFIT) war es, die Behandlungsrealität (real world evidence) in der Diagnostik und der Therapie verscheidener Stadien des PCA (mHSPC, mCRPC) in Deutschland zu erfassen.
Material und Methoden
Im August 2025 erfolgte für 10 Wochen die freiwillige Befragung von Urologen in Deutschland mittels eines standardisierten Fragebogens, welcher via QR-Code abrufbar war. Der Fragebogen umfasste 22 Fragen zur Diagnostik und Therapie verschiedener Stadien des PCa.. Abgefragt wurde u.a. die Anwendung eines mpMRT, Art der Prostatabiopsie inkl. Fusionstechnik, Staging, Therapie des metastasierten hormon-sensitiven PCa (mHSPC) und des metastasierten kastrationsresistenten PCa (mCRPC), molekulare Testungen sowie Arbeitsplatz/Person/Position.
Ergebnisse
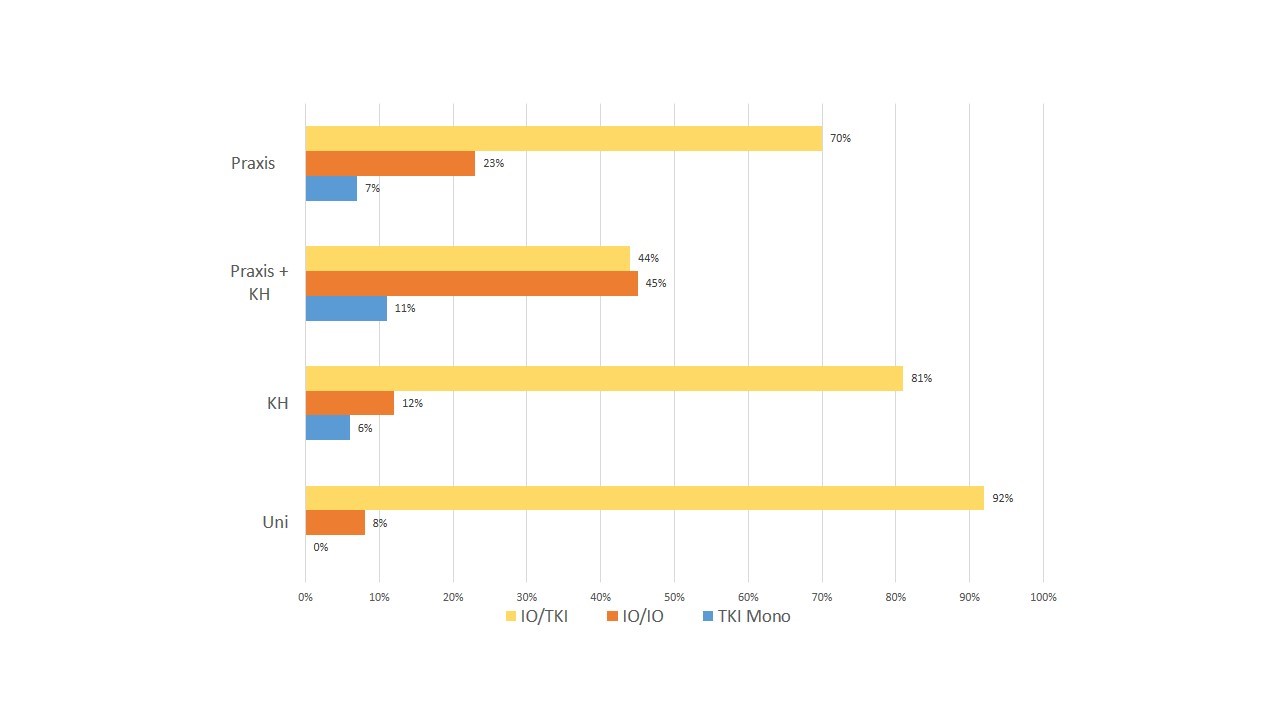
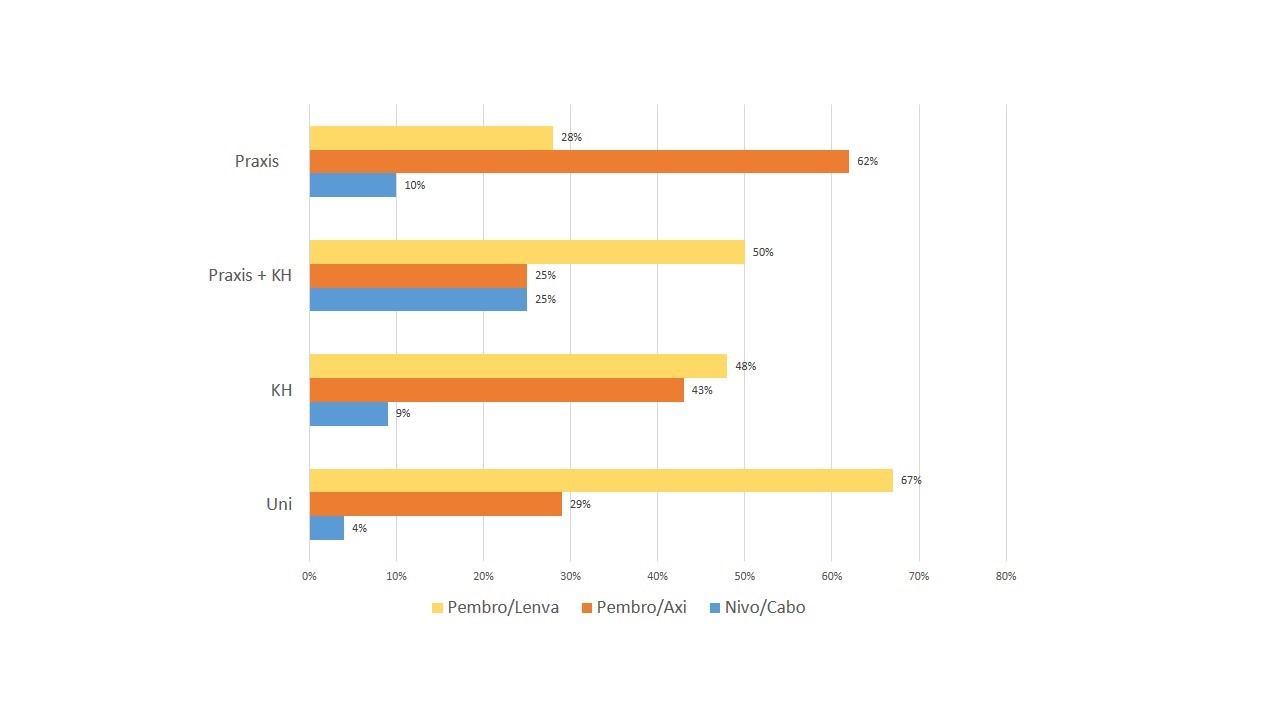
136 Urologen nahmen teil (76% m), 52% arbeiteten in einer Praxis, 48% in einer Hauptabteilung, davon 16% an einer Uniklinik. Ein mpMRT erfolgte häufiger in einer Hauptabteilung (77%), seltener in Praxen (55%). In 50% der Fälle erfolgte die Prostatabiopsie transrektal (dabei 60% in Praxen), in 36% transperineal (vorwiegend an Universitätskliniken 91%). Die Fusionstechnik wurde von 81% durchgeführt, häufiger an Universitätskliniken und Hauptabteilungen (100% bzw. 93%) im Vgl. zur Praxis (59%). Eine Staging-Untersuchung mittels PSMA-PET/CT erfolgt in der Mehrzahl an Universitätskliniken (73%), in der Praxis und den Hauptabteilungen erfolgt vor allem die konventionelle Bildgebung (81% bzw. 75%). Unabhängig vom Arbeitsplatz erfolgte die Therapie des mHSPC in 62% mit der Kombination aus ADT/Apalutamid (ADT/Enzalutamid 16%, ADT/Darolutamid/Docetaxel 10%). Molekulare Testungen führten 50% durch, häufiger an Universitätskliniken (91%) im Vgl. zu Praxen (42%), Die initiale Therapie des mCRPC erfolgte in 31% mit Docetaxel, 29% PARPI/NHT, 18% Switch des NHT und in 4% mit Lutetium.
Schlussfolgerung
Mit der vorliegenden Befragung der DGFIT wurden erstmals in Deutschland systenatisch Real World Daten zur Diagnostik- und Behandlungsrealität des PCa erhoben. Es zeigen sich sowohl in der Diagnostik als auch in der Therapie des PCA deutliche Unterschiede zwischen Praxen und Kliniken. Dies betrifft den Einsatz des mpMRT, die Art der Biopsie, die Art der Staging-Untersuchungen, als auch die molekulare Testung. In der Behandlung des mHSPC ist die Kombination ADT/Apalutamid unabhängig vom Arbeitsplatz etabliert. Eine einheitliche Therapie des mCRPC existiert nicht. Die Gründe für die Unterschiede zwischen Klinik/Praxis (Verfügbarkeit, zusätzliche Kosten für Urologe und Patient etc.) sind bisher unklar und müssen eruiert werden, um in Zukunft eine optimale Behandlung der Patienten zu erreichen.
Verleihung Clinical Science Award 2025
Den Abschluss des Symposiums bildete der Vortrag des CSA-Preisträgers 2025 mit anschließender Preisverleihung. Die DGFIT unterstützt seit ihrer Gründung wissenschaftliche Forschungsprojekte auf dem Gebiet der Immun- und Targeted Therapie. Unter anderem wird jährlich der mit 2.000,00 Euro dotierte Clinical Science Award vergeben.
Mit dem CSA 2025 wurde Dr. Adrian Gottschlich ausgezeichnet für seine Arbeit
Dissection of single-cell landscapes for the development of chimeric antigen receptor T cells in Hodgkin lymphoma

Zusammenfassung
Das Projekt befasst sich mit der Entwicklung neuartiger Immuntherapien für das Hodgkin-Lymphom, eine Krebserkrankung, die vor allem Kinder und junge Erwachsene betrifft. Obwohl heute über 90 Prozent der Patientinnen und Patienten durch intensive Chemotherapie geheilt werden können, leiden viele Betroffene lebenslang unter schweren Spätfolgen. Ziel des Projekts war es daher, gezielte immuntherapeutische Ansätze zu entwickeln, die eine hohe Wirksamkeit mit einer Reduktion langfristiger Toxizitäten verbinden.
Ein zentrales Hindernis für Immuntherapien beim Hodgkin-Lymphom ist das ausgeprägte immunsuppressive Tumormikromilieu, welches die körpereigene Abwehr effektiv lahmlegen kann. Mithilfe von Einzelzellanalysen konnte in diesem Projekt das Molekül CD86 als bislang unterschätztes zentrales Steuerelement dieser Immununterdrückung identifiziert werden. CD86 wird sowohl von den malignen Hodgkin-Zellen als auch von tumorunterstützenden Immunzellen im Tumorumfeld exprimiert und spielt eine Schlüsselrolle in der Hemmung effektiver T-Zell-Antworten.
Auf Basis dieser Erkenntnisse wurden neuartige CD86-gerichtete Immuntherapien entwickelt und umfassend präklinisch untersucht. Neben gezielten Blockadestrategien lag ein besonderer Fokus auf der Entwicklung CD86-gerichteter CAR-T-Zellen. Diese zeigten in präklinischen Modellen eine außergewöhnlich hohe antitumorale Wirksamkeit. Anti-CD86-CAR-T-Zellen führten zu einer schnellen, tiefen und nachhaltigen Eliminierung der Tumorzellen – selbst in stark immunsuppressiven Tumorumgebungen und in Modellen therapieresistenter Erkrankung.
Der hohe therapeutische Effekt beruht auf einem einzigartigen doppelten Wirkmechanismus: Die CAR-T-Zellen zerstören nicht nur direkt die malignen Hodgkin-Zellen, sondern eliminieren gleichzeitig tumorunterstützende Immunzellen im Mikromilieu. Dadurch wird das immunsuppressive Umfeld grundlegend umprogrammiert.
Ein zentrales Element der Studie war außerdem die sorgfältige Sicherheitsbewertung. Die CD86-gerichteten Immuntherapien beeinträchtigten weder die antimikrobielle Immunabwehr noch die Immunantwort auf Impfungen in relevanten präklinischen Modellen. Damit erfüllen sie eine entscheidende Voraussetzung für eine zukünftige klinische Anwendung, insbesondere bei jungen Patientinnen und Patienten.
Die Ergebnisse dieser Arbeit legt die Grundlage für die klinische Weiterentwicklung CD86-gerichteter Immuntherapien für die Therapie von Patienten mit Hodgkin-Lymphomen. Sie eröffnen neue Perspektiven für hochwirksame, zugleich schonendere Behandlungsstrategien – insbesondere für Patientinnen und Patienten mit therapieresistenter Erkrankung oder hohem Risiko für therapiebedingte Langzeitfolgen.
Verleihung des Clinical Science Award 2025 an Dr. Adrian Gottschlich, München
v.l.n.r. Prof. Dr. Michael Siebels (Vorstand DGFIT), Prof. Dr. Elfriede Nößner (Vorstand DGFIT), Dr. Adrian Gottschlich (CSA-Preisträger per Videozuschaltung), Prof. Dr. Christian Doehn (Vorstand DGFIT), Prof Dr. Axel Hegele (Vorstand DGFIT)