Der 25. Urologische Winterworkshop fand unter Leitung von Prof. Martin Kriegmair und Dr. Ralph Oberneder vom 26.01. bis 29.01.2016 im Kongresszentrum Krallerhof in Österreich statt. Wie jedes Jahr wurde mit zahlreichen Vorträgen und Workshops über den aktuellen Forschungsstand der Urologie ein interessantes und vielseitiges Programm geboten.
Die Veranstaltung eines Satellitensymposiums durch die DGFIT im Rahmen des Winter-Workshops in Leogang hat bereits Tradition. Diesmal war es jedoch eine außergewöhnliche Veranstaltung: Nicht nur der Urologische Winterworkshop beging sein Viertel-Jahrhundert Jubiläum, sondern auch die DGFIT hatte etwas Besonderes zu feiern: Die Gesellschaft gibt es jetzt schon seit 15 Jahren. Daher war es eine besondere Freude, dass Prof. Edith Huland, Gründerin und Ehrenmitglied der DGFIT aus Hamburg, einen Überblick über 15 Jahre Immuntherapie gab. Das Symposium fand unter Leitung von Prof. Dr. M. Siebels, München, und Prof. Dr. H. Heinzer, Hamburg statt.
Die Vorträge zu aktuellen Themen des Nierenzellkarzinoms werden im Folgenden kurz dargestellt:
Frau Prof. Dr. Edith Huland, Hamburg

Frau Prof. E. Huland brachte einen Überblick über die alte und neue Bedeutung von Interleukin-2 (IL-2) in den letzten 15 Jahren:
Immuntherapie ist ein wesentlicher Schlüssel zur Heilung von Krebs- und Viruserkrankungen. IL-2, das Immunhormon, welches das Immunsystem des Patienten fit macht, um Tumorzellen zu vernichten, bekommt heute genau deshalb wieder neue Anerkennung (2014 Muhitch et al. High-dose IL-2 for metastatic renal cell carcinoma: can the first antitumor immunotherapy be reinvented? Immunotherapy 6, 955). Steven Rosenberg berichtet aktuell von einer Patientin mit metastasiertem Melanom, die 1984 durch IL2 eine komplette Remission erfahren hat und nachweislich mehr als 29 Jahren tumorfrei ist. (2014 Rosenberg: IL-2 The First Effective Immunotherapy for human Cancer. J Immunol, 192, 5451). Das immunologische Potential von IL-2 wird gerade (wieder) entdeckt. Wer mit einem metastasierten Nierenzellkarzinom (mRCC) Heilung sucht, hat auch heute keine andere Alternative, so Hanzly: „Patients with mRCC have poor survival, and the only treatment option with durable remissions and proven track record of cure in this otherwise lethal disease is HDIL-2 immunotherapy.“ (2014 Hanzly High-dose Interleukin-2. Therapy for mRCC: A Contemporary Experience. Urology 83: 1129e1134).
Der Grund für das Schattendasein von IL-2 in den letzten Jahren ist die hohe Toxizität der zugelassenen Applikationsformen (Infusion oder Injektion von IL-2). Fieber, Schüttelfrost und massive Gewebeödeme durch das „Vasculary Leakage Syndrome“ erlauben keine Anwendung beim „typischen“ älteren Tumorpatienten. Es werden daher seit langem andere Anwendungs-Wege gesucht, zum Beispiel der Einsatz von Zelltherapien mit IL-2 stimulierten Zellen oder mit IL-2 stimulierten Immunzellen, die mit chimärischen Antigen Rezeptoren genetisch verändert sind (2014 Rosenberg Zitat siehe oben). Ein eleganter Weg zur Reduktion der Nebenwirkungen sind andere Applikationsformen. Ein Beispiel ist die Inhalation von IL-2 (1993 Huland et al: Interleukin-2 by inhalation: Local therapy for metastatic renal cell cancer, J Urol 147, 344). Weltweit wurde in der Literatur inzwischen von ca. 800 Patienten – überwiegend mit mRCC, manche mit Melanom und weitere mit anderem Primärtumor wie Brustkrebs oder Ovarialkarzinom – berichtet, die die inhalative IL-2 Therapie gut vertrugen und erfreuliche Hinweise lieferten für die Effektivität dieser Therapie bis hin zu kompletter Tumorremission in der Lunge bei alleiniger inhalativer Applikation. Die jüngste Publikation zur Inhalation von IL-2 stammt aus San Francisco (2014 Posch et al Low-dose inhalation of IL-2).
Die lokale Anwendung von IL-2 z.B. durch Instillation in die Harnblase bei Blasenkrebs, durch Inhalation in die Lunge bei pulmonalen Metastasen, durch lokale direkte Injektion in Tumorbereiche orientiert sich am physiologischen Wirkmechanismus und verändert das Nebenwirkungsprofil von Interleukin-2 substantiell. Das natürliche IL-2 steht schon lange nicht mehr zur Verfügung. Um robustere Varianten von IL-2 für die Arzneimittelbehandlung zu entwickeln, haben Huland und Kollegen daher 2006 eine Orphan Designation bei der EMA für das pulmonal metastasierte Nierenzellkarzinom erarbeitet und setzen aktuell diese Arzneimittelentwicklung um. Derzeit werden mit dem innovativen IL-2 in neuen Formulierungen bei Pferden mit Papilloma Virus-induzierten Tumoren tiertoxikologische Untersuchungen mit erfreulich guten Ergebnissen durchgeführt. Das innovative IL-2 steht für Forschung und Entwicklung zur Verfügung. Die Entwicklung eines innovativen, robusten IL-2 Arzneimittels für Spezialapplikationen eröffnet kuratives Potential für Patienten mit dringendem Bedarf und bietet uns allen neue Forschungs- und Entwicklungsansätze, um das Potential von IL-2 auszuschöpfen.
Prof. Dr. Christian Doehn, Lübeck

Herr Prof. Dr. C. Doehn, Koordinator der aktuellen S3 Leitlinie, gab einen Überblick über Diagnostik, Therapie und Nachsorge beim Nierenzellkarzinom:
Im September 2015 wurde die erste S3-Leitlinie zur Diagnostik, Therapie und Nachsorge des Nierenzellkarzinoms fertiggestellt und online publiziert (http://leitlinienprogramm-onkologie.de/Nierenzellkarzinom.85.0.html). Die Leitlinie entstand unter der Federführung der Deutschen Gesellschaft für Urologie (DGU) sowie der Deutschen Gesellschaft für Hämatologie und Onkologie (DGHO) und wurde von Vertretern 30 verschiedener Fachgesellschaften bzw. Fachgruppen erarbeitet. Sie richtet sich an Ärztinnen und Ärzte der hausärztlichen Versorgung, niedergelassene und klinisch tätige Urologen, Onkologen etc., Pflegekräfte und Therapieberufe, Organisationen der Patientenberatung, Selbsthilfegruppen sowie Kostenträger.
Inhaltlich wird hinsichtlich der Tumorsituation vor allem auf Pathologie und Staging des Nierenzellkarzinoms eingegangen. Bei der operativen Therapie werden die verschiedenen Möglichkeiten des organerhaltenden Vorgehens behandelt. Ferner wird ein individuelles Nachsorgeschema vorgestellt. Beim mRCC geht es neben den verschiedenen medikamentösen Ansätzen um die mögliche Rolle operativer und strahlentherapeutischer Verfahren. Eine Übersicht zu supportiven Maßnahmen sowie komplementären und palliativmedizinischen Aspekten komplettiert die Leitlinie. Im Sommer 2016 wird ein Amendment den aktuellen Entwicklungen der medikamentösen Therapie Rechnung tragen. Die Leitlinie hat insgesamt eine Gültigkeit bis zum Herbst 2018.
Prof. Dr. Michael Siebels, München

Herr Prof. Dr. M. Siebels berichtete über den aktuellen Stand bei der Therapie des Nicht-klarzelligen Nierenzellkarzinoms (RCC):
Während sich die operative Therapie des lokal begrenzten Nicht-klarzelligen RCC nicht von der des klarzelligen RCC unterscheidet und gute Heilungsergebnisse erzielt, ist die Therapie des Nicht-klarzelligen metastasierten RCC (mRCC) trotz der vielen neuen zugelassenen Therapieformen immer noch ein großes Problem. Dies schlägt sich auch in den bisher publizierten internationalen Leitlinien nieder. Leitlinien wie die der EAU (European Association Urology), der ESMO (European Society Medical Oncology), der NCCN (National Comprehensive Cancer Network) geben entweder keine Hinweise zur Therapie des Nicht-klarzelligen mRCC oder übernehmen dafür die Therapie vom klarzelligen mRCC. In der aktuellen deutschen S3 Leitlinie wird die Therapie des Nicht-klarzelligen mRCC ebenfalls ausgeblendet, soll aber im kommenden Amendment aufgegriffen werden. Ein Problem ist sicherlich, dass sich die meisten Studien mit dem sehr viel häufigeren klarzelligen mRCC beschäftigten. Ein weiteres Problem ist die uneinheitliche histologische Einordnung. Dies soll sich in Zukunft mit der neuen ISUP Einteilung ändern, die auch die neue WHO Klassifikation 2016 des RCC verändern wird. Bis sich jedoch speziell auf das Nicht-klarzellige mRCC zugeschnittene Therapien entwickeln, wird noch einige Zeit vergehen. Patienten mit Nicht-klarzelligem mRCC sollten, wenn möglich, an den (wenigen) Studien teilnehmen. Derzeitige Therapie-Empfehlungen (mTOR Inhibition, VEGF Blockade) richten sich zwar (noch) am klarzelligen mRCC aus, sind aber scheinbar bei den verschiedenen Formen der Nicht-klarzelligen RCCs nicht sehr wirksam. Weitere Studien mit etablierten Substanzen sind daher eher nicht zielführend. Die Entwicklung neuer Therapien mit Hilfe von Biomarkern oder aufgrund neuer histopathologischer Entwicklungen müssen unterstützt werden. Der gerade sich in der Zulassung befindliche Checkpoint-Inhibitor Nivulomab scheint eventuell auch eine neue Therapieoption beim Nicht-klarzelligen mRCC zu sein, womit erneut die große Bedeutung der Immuntherapie beim mRCC bestätigt wird.
Dr. Zoltan Varga, Sigmaringen

Herr Dr. Z Varga, Chefarzt aus Sigmaringen, gab seine Einschätzung darüber ab, was sich durch die Zulassung von Nivolumab in der Therapie des mRCC ändern wird:
Die Prognose des fortgeschrittenen RCC ist auch in der Ära der zielgerichteten Therapie mit Tyrosinkinase-Inhibitoren ernst. Die 5 Jahre Überlebenszeit liegt bei 10 bis 15 %. Tumore entwickeln unterschiedliche Escape-Mechanismen, um ihrer Zerstörung durch eine systemische Therapie oder durch das Immunsystem zu entgehen.
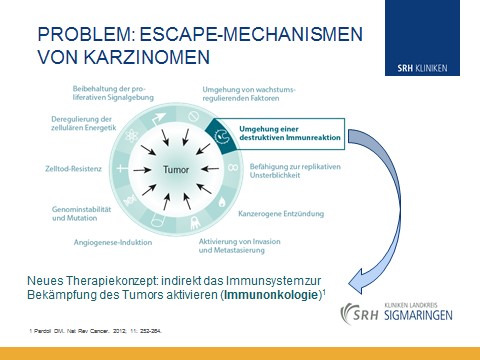
Insbesondere bei der antitumoralen Immunantwort gibt es Ansatzpunkte, die der Tumor nutzt, um die Immunreaktion abzuschalten. Hier setzt der Mechanismus der Checkpointinhibitoren, zu dem auch Nivolumab zählt, an. Die Substanzen verteidigen die Immunreaktion vor Angriffen durch den Tumor. In der Zulassungsstudie Checkmate 025 konnte bei der Zweitlinientherapie gegenüber Everolimus ein signifikanter Vorteil im medianen Gesamtüberleben von 5,4 Monaten bei guter Verträglichkeit aufgezeigt werden.
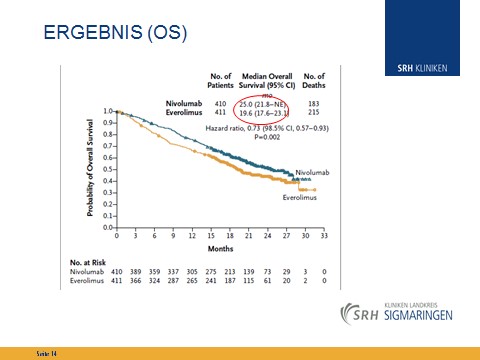
Die Zulassung in Deutschland in der Zweitlinientherapie des Nierenzellkarzinoms für Nivolumab wird im Frühjahr 2016 erwartet. Die Substanz hat in den bisherigen Studien bei einem Teil der Patienten langfristige Remissionen gezeigt, Synergieeffekte mit anderen Systemtherapien werden postuliert. Es besteht die Hoffnung, dass zukünftig das fortgeschrittene Nierenzellkarzinom in eine „chronische“ Erkrankung, wenigstens bei einem Teil der Betroffenen, überführt werden kann.
Weitere Informationen unter: www.winterworkshop.de













